INTRODUÇÃO
Chamamos de encefalopatia hepática um conjunto de alterações neuropsiquiátricas associadas a disfunção do fígado (do fígado = hepática). Essas alterações variam de sintomas mínimos (observados apenas em testes) até alterações de comportamento e confusão mental e, se não tratada, avança com graus progressivos de sonolência até o coma.
De modo bem simplificado, a encefalopatia ocorre quando o fígado não consegue impedir que toxinas provenientes da dieta e da ação das bactérias intestinais cheguem ao cérebro, causando lesão cerebral. Isso pode ocorrer na hepatite aguda grave, quando o fígado perde a capacidade de metabolizar essas toxinas, ou em casos quando há desvio de sangue rico em toxinas direto para o cérebro sem passar pelo fígado, como após procedimentos cirúrgicos ou radiológicos para o tratamento de hipertensão portal.

Na maioria das vezes, a encefalopatia ocorre na cirrose hepática, pelos dois mecanismos acima. É uma complicação relativamente comum e grave da cirrose avançada, sendo a segunda principal causa de internação hospitalar desses pacientes (logo após a ascite). Sinais leves de encefalopatia podem ser observados em até 70% dos cirróticos, sendo que 30-45% dos portadores de cirrose vão apresentar sintomas evidentes de encefalopatia em algum momento. Sintomas severos que justifiquem internação indicam doença mais grave, sendo importante observar que a hospitalização por encefalopatia significa uma chance de 41% de sobrevivência em 1 ano, ou de 23% em 3 anos.
Além disso, há evidências de que a encefalopatia hepática cause danos progressivos e irreversíveis ao cérebro, devendo ser identificada e tratada para evitar limitações e sintomas neurológicos a longo prazo.
COMO A ENCEFALOPATIA OCORRE
O fígado é um órgão aparentemente simples, mas na verdade é altamente complexo. Apesar de ter um pequeno número de células diferentes, é responsável por mais de 500 funções, incluindo o metabolismo de açúcares e gorduras, a produção de proteínas essenciais, a transformação de alimentos e a eliminação de toxinas, sendo essa última a relacionada a encefalopatia.
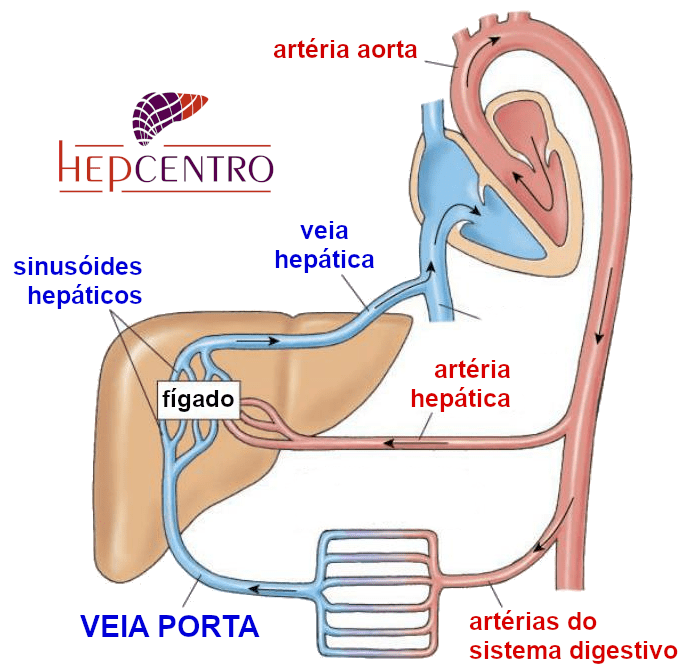
Para se ter uma ideia da importância do fígado no metabolismo basta observar como é a circulação do sangue: todo o sangue que sai do intestino, rico em nutrientes e toxinas, se junta em uma única veia, a veia porta, que distribui o sangue pelo fígado. Em relação à encefalopatia, a toxina mais importante é a amônia, que é produzida pelas bactérias intestinais.

Chegando no fígado, o sangue rico em amônia sai do ramo da veia porta (PV) e passa pelos sinusoides, de onde as toxinas são retiradas pelos hepatócitos (principais células do fígado) antes de chegarem na veia central (CV), que leva o sangue sem toxinas para o resto do organismo, incluindo o cérebro. A amônia é metabolizada mais na chamada zona 1, logo no começo do trajeto entre a tríade portal (PT, composta de ramos da veia porta, artéria hepática e ducto biliar). Medicamentos são metabolizados mais na zona 3, próximo da veia central (fonte).
O fígado tem uma capacidade fantástica de se regenerar. Em estudo onde foi retirado 2/3 do fígado (cirurgia que pode ser realizada após trauma ou para retirada de tumores), observou-se que o processo de regeneração começa 5 minutos após o procedimento, e o fígado humano recupera o seu peso anterior entre 8 e 15 dias. Mas é claro que tudo tem limite. Se há uma infecção grave no fígado, ou uma intoxicação como a causada por tentativa de suicídio por paracetamol, a destruição de hepatócitos pode ultrapassar a capacidade de fígado de se regenerar, fazendo com o que órgão não consiga desempenhar as suas funções. Chamamos isso de hepatite fulminante, e o surgimento de encefalopatia hepática logo nos primeiros dias ou semanas é a sua principal característica, que indica altíssima mortalidade.
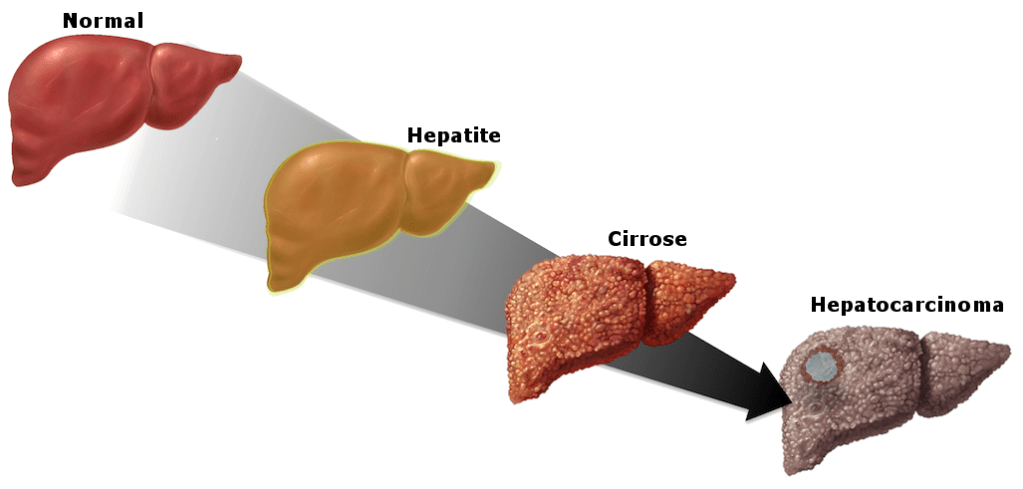
A maioria dos casos de encefalopatia hepática não ocorre de forma tão abrupta, mas como consequência de um processo lento. Quando doenças do fígado causam lesão crônica dos hepatócitos, ao longo de décadas, as células vão se regenerando e formando cicatrizes. Essas cicatrizes vão crescendo até formarem nódulos e distorcer o fígado, chegando ao ponto que chamamos de cirrose. Na cirrose a encefalopatia ocorre por dois mecanismos principais: a perda da capacidade de regeneração (chega um momento em que os hepatócitos não conseguem mais se multiplicar como antes), levando à perda de função, e o desvio de sangue direto da veia porta para a circulação geral, decorrente da hipertensão portal.
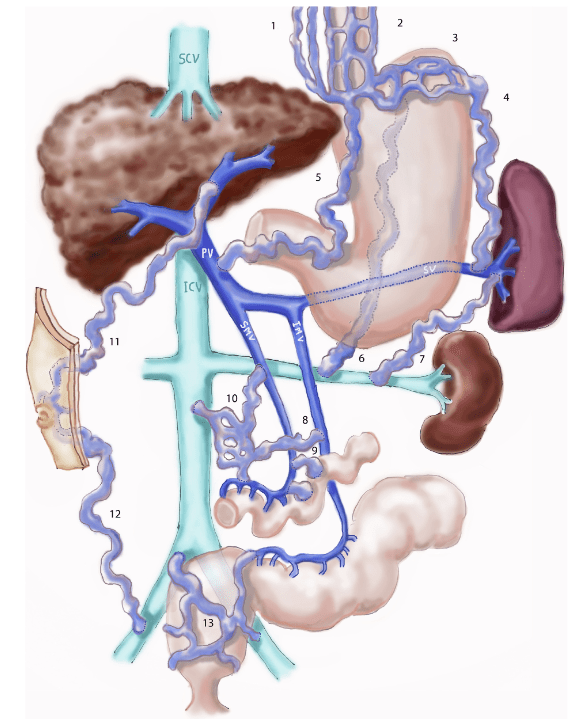
No fígado normal, o sangue fui bem da veia porta até as veias centrais e de lá para as veias hepáticas e a circulação geral. À medida que uma doença (hepatite, lesão pelo álcool, etc.) evolui para a cirrose, o fluxo de sangue fica mais difícil tanto pela inflamação quanto pela presença de cicatrizes, aumentando a pressão na veia porta. Essa hipertensão portal leva a dilatação tanto da veia porta como das veias que levam a ela, causando aumento do baço (esplenomegalia), acúmulo de água no abdome (ascite), varizes esofágicas e, algumas vezes, uma ou mais pequenas veias que iam direto do intestino ou do baço para a circulação geral, causando um “curto circuito” (chamado “shunt portosistêmico) e levando o sangue repleto de neurotoxinas direto para o cérebro.
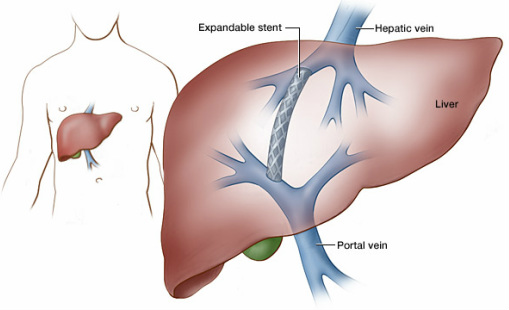
Em algumas situações, é necessário criar shunts artificiais par reduzir a hipertensão portal. Em portadores de esquistossomose hepatoesplênica, onde a função do fígado geralmente é normal mesmo na doença avançada, a hipertensão portal pode levar a hemorragias pelas varizes e ascite de difícil controle, sendo necessário desviar sangue da veia porta para reduzir a pressão, o que geralmente era realizado através de cirurgia. Mesmo na cirrose, algumas vezes é necessário o mesmo, sendo realizado um procedimento radiológico chamado shunt portossistêmico transjugular intrahepático (TIPS).
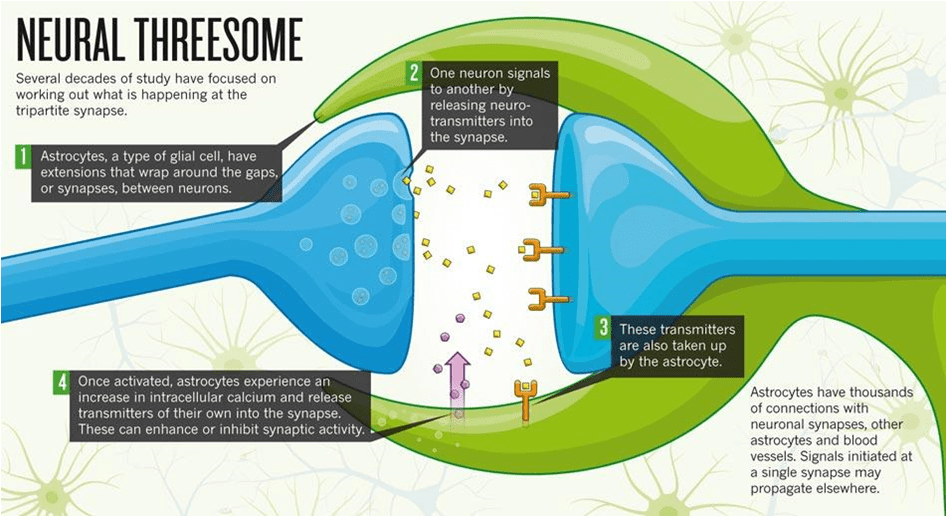
Independente do mecanismo, as neurotoxinas (amônia, manganês e outras) chegam ao cérebro, onde vão afetar principalmente os astrócitos, células responsáveis por manter e proteger os neurônios e auxiliar nas suas funções, incluindo retirar neurotransmissores usados das sinapses nervosas. No caso das hepatites fulminantes, os astrócitos incham e podem até causar hipertensão intracraniana intracraniana e óbito. Na cirrose e nas demais condições crônicas, esse inchaço é menos evidente ou não ocorre, surgindo alterações na célula chamadas de “astrócito de Alzheimer tipo II”. Não há ainda um consenso sobre o que exatamente acontece no cérebro, mas os astrócitos deixam de funcionar normalmente, o que causa um acúmulo de neurotransmissores. Além disso, a amônia, manganês, GABA e outras neurotoxinas pode agir como falsos neurotransmissores, estimulando ou inibindo neurônios ao acaso.
SINTOMAS
De modo geral, a encefalopatia surge de forma praticamente imperceptível, pode passar por uma fase de agitação, alteração de personalidade e confusão mental e depois evolui com sonolência inicialmente diurna, contrastando com insônia noturna (o que chamamos de inversão de ciclo sono-vigília) que vai piorando até letargia e coma. O espectro de sintomas progressivos é melhor resumido na classificação mais utilizada de graus de encefalopatia hepática de West-Haven, mas deve-se levar em consideração de que nem sempre os sintomas todos são observáveis e que frequentemente também não surgem nessa ordem.
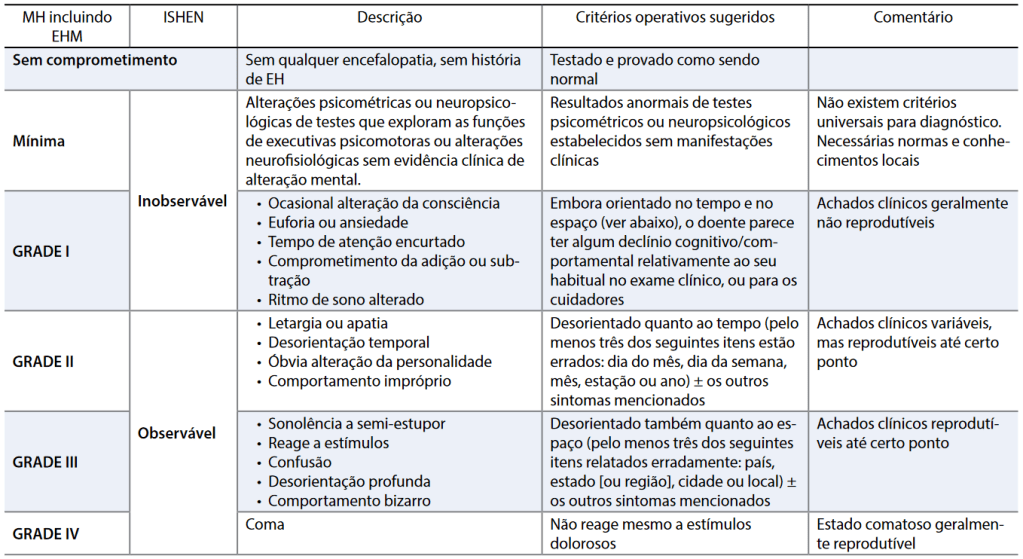
Encefalopatia hepática mínima é uma condição de importância porque, apesar da pessoa ter raciocínio, memória, linguagem e funções motoras aparentemente normais, já há perda na capacidade de concentração e no tempo de resposta. Isso pode significar já uma incapacidade de dirigir e operar máquinas, mesmo sem nenhum sintoma aparente. Seria bom se existisse algum teste laboratorial ou teste simples para diagnosticar essa condição, mas ele não existe. Os testes neuropsiquiátricos usados para isso (testes numéricos ou de associação de palavras e cores como o teste stroop) são difíceis de interpretar porque há variação de pessoa para pessoa e os resultados podem depender de outros fatores além de encefalopatia. Os testes psicométricos também são difíceis de interpretar e utilizar na prática.
No grau I, as alterações podem ser discretas demais para serem identificados, mas podem chamar a atenção de familiares ou de cuidadores mais atentos. Até esse ponto, chamamos a encefalopatia de “oculta”.

Outro sinal clínico que não ocorre em todos os pacientes mas que em alguns é muito claro é o fetor hepaticus, um hálito adocicado intenso pela presença de tióis. Eles são muitas vezes descritos como cheiro de alho, mas para mim parecem mais com banana madura demais. Para ter uma ideia da intensidade, tióis são usados para dar o odor no gás de cozinha (para ser detectado em casos de vazamento bem antes de atingir concentração suficiente para queimar) e no borrifo de gambás.
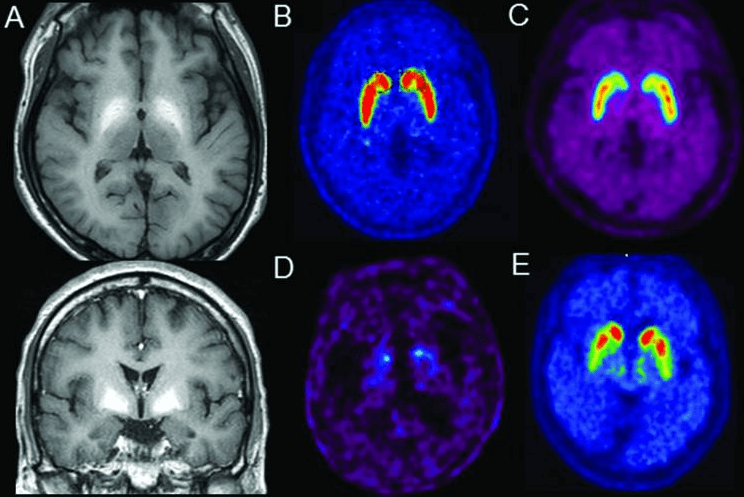
Em todo paciente com cirrose que apresenta sintomas neurológicos, duas considerações devem ser feitas: uma é que outras condições podem estar presentes e confundir o quadro clínico. Portadores de doença de Wilson tem sintomas neurológicos específicos, que podem estar associados ou não a encefalopatia. Pacientes com doença hepática gordurosa tem maior risco de doenças cardiovasculares. Alcoólatras podem apresentar demência alcoólica, síndrome de Wernicke-Korsakoff e síndrome de abstinência. Outra consideração é que, se não for possível a avaliação por neurologista em todos os pacientes, ela deve ser realizada em todos os paciente com sintomas atípicos, especialmente nos pacientes com alucinações, convulsões e sintomas motores.
O diagnóstico da encefalopatia hepática é feito pelos sintomas e exame físico. Exames laboratoriais, eletroencefalograma e exames de imagem geralmente são úteis apenas para descartar outras doenças neurológicas. A ultrassonografia com Doppler do abdome pode mostrar shunts portosistêmicos. A dosagem de amônia tem utilidade limitada, já que a amônia elevada pode não estar relacionada a sintomas neurológicos. Por outro lado, a dosagem normal pode ajudar a descartar encefalopatia hepática. Infelizmente, na prática é difícil encontrar laboratórios que realizem esse exame.
EVOLUÇÃO E FATORES DESENCADEANTES
Em teoria, a encefalopatia hepática causada pela cirrose surgiria quando o conjunto de perda de função hepática e shunts portossistêmicos (curto circuitos entre a veia porta e a circulação geral) chegasse ao ponto em que há amônia e outras neurotoxinas suficiente no cérebro para desencadear sintomas, e esses piorariam gradualmente à medida que a doença do fígado avançasse. Na prática, no entanto, temos pacientes com sintomas que aparecem e desaparecem, e a partir de um certo ponto melhoram e pioram, mas não desaparecem mais. Isso acontece porque, além da evolução natural da doença do fígado, o aparecimento e a piora dos sintomas estão geralmente relacionados a fatores desencadeantes:
- Infecções podem causar piora ou desencadeamento da encefalopatia por vários mecanismos; na minha experiência, devemos sempre descartar pneumonia, infecção urinária e celulite do abdome e das pernas;
- Hemorragia gastrointestinal, seja ela causada por rompimento de varizes esofágicas ou não, pode desencadear diretamente encefalopatia pois o sangue digerido gera amônia; além disso, hemorragias predispõe a infecções como a peritonite bacteriana espontânea, a sofrimento e insuficiência renal e a efeitos colaterais de transfusões
- Insuficiência renal, que pode ser crônica mas também pode ser reversível se causada por medicamentos, infecções urinárias ou desidratação;
- Constipação aumenta a produção e absorção de amônia, sendo um fator desencadeante muito comum e facilmente tratável;
- Diuréticos podem desencadear encefalopatia por si só, mas principalmente se levam a redução de potássio e alcalose; a encefalopatia pelos diuréticos pode ser difícil de reconhecer e tratar principalmente se o paciente tiver ascite e necessite dos medicamentos
- Medicamentos como opióides, anti psicóticos, anti depressivos e benzodiazepínicos podem desencadear e piorar a encefalopatia hepática; isso é especialmente comum quando o paciente apresenta inversão do ciclo sono-vigília pela encefalopatia, procura atendimento médico para tratar a insônia noturna e recebe receita de benzodiazepínico (para ser justo, muitas vezes isso acontece quando o paciente não sabe que tem cirrose ou não menciona para o médico);
- Sobrecarga de proteínas que vai aumentar a produção de amônia no intestino
CLASSIFICAÇÃO
Existe uma classificação de encefalopatia hepática proposta pela EASL (Associação Europeia para o Estudo do Fígado) que é interessante porque resume bem todo o texto anterior:
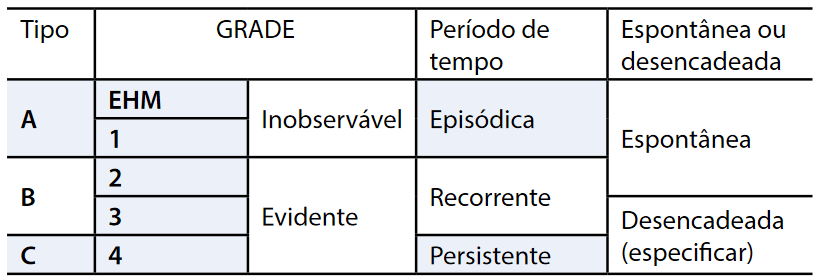
Segundo essa classificação, um paciente poderia ser descrito como tendo “EH tipo C, grau 2, episódica por celulite”.
TRATAMENTO
O tratamento da encefalopatia hepática varia muito da situação. Paciente com sintomas devido a hepatite fulminante, por exemplo, são candidatos a transplante hepático de urgência (entram como prioridade na fila), necessitam de Unidade de Tratamento Intensivo e, como tem mais inchaço dos astrócitos do que na doença crônica, precisam de medicamentos específicos para reduzir o inchaço. Pacientes com encefalopatia e abuso de álcool, especialmente naqueles com hepatite alcoólica grave, precisam de tratamento específico e correm alto risco de síndrome de abstinência e Wernicke-Korsakoff, devendo receber tiamina e controlar a agitação com haloperidol ao invés de benzodiazepínicos, que são o tratamento usual.

Não cabe nesse texto discutir todas as possibilidades, então vamos nos concentrar no que é a situação da maioria dos pacientes com encefalopatia hepática: portadores de cirrose com sintomas episódicos, recorrentes ou persistentes leves a moderados. O seguintes tratamentos são, muitas vezes, complementares e podem ser associados. A escolha depende muito da experiência do médico, da gravidade do quadro e da disponibilidade de cada opção.
Tratar fatores desencadeantes
Cerca de 90% dos casos de encefalopatia episódica ou recorrente conseguem ser controlados com facilidade apenas tratando o fator desencadeante: antibióticos para infecções, laxativos ou lavagem intestinal para constipação, retirar diuréticos e benzodiazepínicos e hidratação na insuficiência renal. Por isso que reconhecer e tratar essas condições é fundamental. Todo paciente que inicia ou piora a encefalopatia deve entrar em contato com o seu médico ou procurar pronto socorro assim que possível, ao invés de esperar para ver se passa ou tratar por conta própria em casa.
Dieta
A maioria dos paciente com encefalopatia foi o será orientada a retirar carne animal da dieta em algum ponto. Isso porque a proteína animal gera mais amônia produzida pela flora intestinal, portanto essa orientação foi por muito tempo o tratamento inicial prescrito para todos os pacientes que iniciavam encefalopatia e muitas vezes a dieta era mantida para prevenir novas crises.

O que se observou ao longo dos anos é que, mesmo sem dieta, a maioria dos portadores de cirrose desenvolve sarcopenia, que é a perda de massa muscular. Há vários mecanismos para que isso aconteça no cirrótico, mas a dieta restritiva acelera em muito essa perda. Além do simples fato de que a sarcopenia em si piora a qualidade de vida e aumenta a mortalidade na cirrose, sabemos que os músculos ajudam a retirar o excesso de amônia do sangue, e músculos atrofiados não conseguem fazer isso, dificultando ainda mais o tratamento. Por esses motivos, a maioria dos pesquisadores não recomenda mais a dieta restritiva, preferindo basear o tratamento da encefalopatia em outras estratégias, ou no máximo restringir por poucos dias apenas.
Laxativos
O simples ato de esvaziar o intestino grosso, reduzindo a quantidade de fezes e bactérias que produzem amônia já ajuda na encefalopatia e é especialmente útil nos pacientes cujos sintomas foram desencadeados pela constipação. Por esse motivo a lavagem intestinal é muito prescrita em pacientes internados.
A lactulose (lactulona, duphalac, farlac, pentalac, lactuliv, inlact) e o lactilol (imolac) são açúcares não absorvíveis que chegam até o intestino grosso e são transformado pelas bactérias em ácido lático e outros ácidos orgânicos. Esses compostos deixam o conteúdo intestinal mais ácido, que é um ambiente ruim para as bactérias produtoras de amônia, transforma a amônia (NH3) que seria absorvida pela mucosa intestinal em amônio (NH4+), que não é absorvível e ainda esvazia o intestino. A dose inicial costuma ser de 30 mL para a ambos, geralmente ajustando-se a dose para alcançar 2 a 3 evacuações ao dia, mas o uso pode ser limitado por diarreia e cólicas.
Antibióticos
Podemos usar antibióticos para reduzir a quantidade de bactérias produtoras de amônia no intestino. Como são usados por longos períodos, devem ser seguros e também não tornar as bactérias multirresistentes, o que dificultaria o tratamento de qualquer infecção no cirrótico. Até recentemente no Brasil, o único antibiótico que encaixava nesse perfil era a neomicina, com dose inicial de 250 mg de 2 a 4 vezes ao dia, até o máximo de 4 gramas por dia. O problema é que a longo prazo corre o risco de causar lesão renal e nos ouvidos.
Recentemente tivemos finalmente a aprovação do uso de rifaximina (Xifaxan), na dose de 400 mg 3 vezes ao dia. É um antibiótico não absorvível, que portanto só afeta as bactérias intestinais sem risco de efeitos colaterais em outros órgãos. Também parece destruir mais bactérias patogênicas e preservar a flora normal. É usado na Europa há mais de 20 anos inicialmente para outras situações, mas se mostrou muito eficaz na encefalopatia hepática, melhor até que a lactulona. Pode ser usado nas crises ou continuamente para evitar crises, mostrando-se eficaz também na encefalopatia mínima.
Suplementos
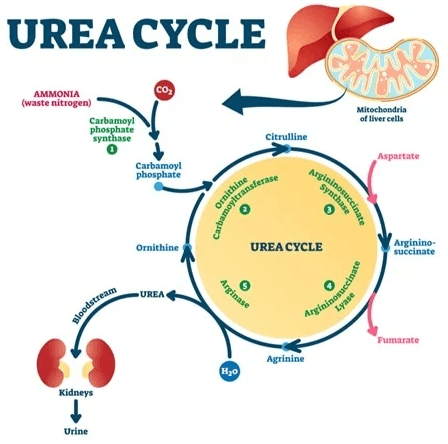
O suplemento L-ornitina L-aspartato, ou LOLA (Hepa-Merz) é um sal estável com dois aminoácidos que são usados na reação química chamada ciclo da ureia. A suplementação com 1 ou 2 envelopes ao dia estimula o ciclo e reduz a quantidade de amônia, ajudando no tratamento da encefalopatia. Tem ainda a vantagem de ajudar a reverter a sarcopenia (perda da massa muscular).
A deficiência de zinco é comum em portadores de cirrose, e a sua suplementação, mesmo em pacientes com zinco normal, poderia ajudar a estimular o ciclo da ureia e auxiliar o tratamento da encefalopatia hepática. Os resultados em pesquisas, no entanto, não são claros.
Outros medicamentos
O fenibutirato de glicerol (GPB) foi desenvolvido para tratar doenças genéticas que afetam o ciclo da ureia. Ele se liga com a glutamina e é excretado na urina levando nitrogênio. É uma opção por ter mecanismo de ação diferente dos demais, mas sua disponibilidade é limitada.
Transplante hepático
Assim como na maioria das complicações da cirrose, o transplante geralmente melhora os sintomas de encefalopatia hepática. Infelizmente, estudos mostram que parte dos danos causados pelas neurotoxinas são permanentes. Pacientes submetidos a transplante e que tiveram encefalopatia antes da cirurgia têm piora função cerebral do que os que não tiveram. Isso reforça a necessidade de diagnosticar e tratar a doença de forma mais agressiva e com medicamentos de uso contínuo, ao invés de apenas em crises, em pacientes que já tiveram algum sinal de encefalopatia.
BIBLIOGRAFIA
- Encefalopatia hepática na doença hepática crónica: 2014 Norma de Orientação da Associação Europeia para o Estudo do Fígado e Associação Americana para o Estudo de Doenças do Fígado. J Hepatol (2014), http://dx.doi.org/10.1016/j.jhep.2014.05.042 (link).
- Wolf, DC. Hepatic Encephalopathy. In Medscape. Acessado em junho de 2021 (link).
- Romeiro, Fernando G. et al. Acquired hepatocerebral degeneration and hepatic encephalopathy: correlations and variety of clinical presentations in overt and subclinical liver disease. Arquivos de Neuro-Psiquiatria [online]. 2011, v. 69, n. 3 [Accessed 13 June 2021] , pp. 496-501.
- Shin HW, Park HK. Recent Updates on Acquired Hepatocerebral Degeneration. Tremor Other Hyperkinet Mov (N Y). 2017;7:463. Published 2017 Sep 5. doi:10.7916/D8TB1K44
- Traub J, Bergheim I, Eibisberger M, Stadlbauer V. Sarcopenia and Liver Cirrhosis-Comparison of the European Working Group on Sarcopenia Criteria 2010 and 2019. Nutrients. 2020;12(2):547. Published 2020 Feb 20. doi:10.3390/nu12020547
- Ebadi M, Bhanji RA, Mazurak VC, Montano-Loza AJ. Sarcopenia in cirrhosis: from pathogenesis to interventions. J Gastroenterol. 2019 Oct;54(10):845-859. doi: 10.1007/s00535-019-01605-6. Epub 2019 Aug 7. PMID: 31392488; PMCID: PMC6759678
- Acharya, Chathur1; Bajaj, Jasmohan S.1 Current Management of Hepatic Encephalopathy, American Journal of Gastroenterology: November 2018 – Volume 113 – Issue 11 – p 1600-1612 doi: 10.1038/s41395-018-0179-4
- Rose, Christopher F. et al. Hepatic encephalopathy: Novel insights into classification, pathophysiology and therapy. Journal of Hepatology, Volume 73, Issue 6, 1526 – 1547 2020
Artigo criado em: 16/06/2021
Última atualização em: 16/06/2021

