INTRODUÇÃO E EPIDEMIOLOGIA
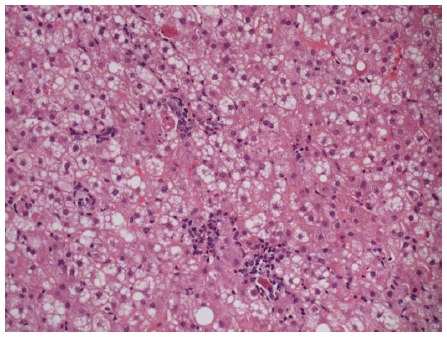
Hepatite C é a inflamação do fígado causada pela infecção pelo vírus da hepatite C (VHC ou HCV), transmitido através do contato com sangue contaminado. Essa inflamação ocorre na maioria das pessoas que adquire o vírus e, dependendo da intensidade e tempo de duração, pode levar a cirrose e câncer do fígado. Ao contrário dos demais vírus que causam hepatite, o vírus da hepatite C não gera uma resposta imunológica adequada no organismo, o que faz com que a infecção aguda seja menos sintomática, mas também com que cerca de 75% das pessoas que se infectam se tornem portadores de hepatite crônica, com suas consequências a longo prazo.

Estima-se que pouco menos de 1% da população mundial, ou de 69-71 milhões de pessoas, sejam portadores de hepatite C crônica, mas os números felizmente estão menores a cada ano. Chegou a ser até recentemente a principal causa de transplante hepático em países desenvolvidos e responsável por 60% das hepatopatias crônicas.
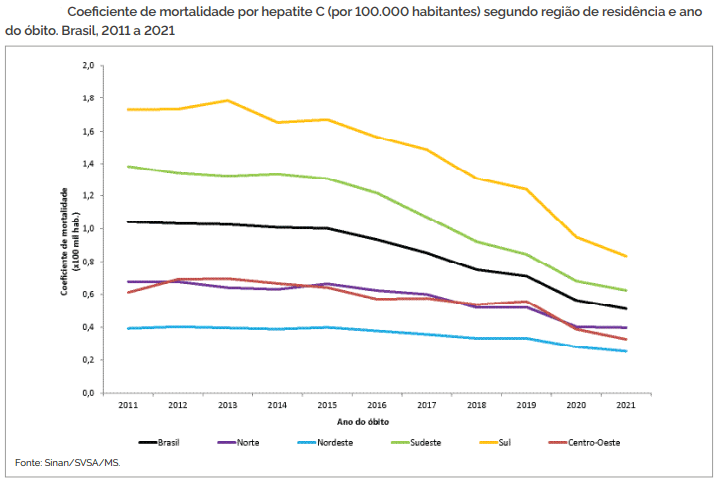
No Brasil, refletindo medidas de controle da transmissão e tratamento dos infectados, observamos uma clara queda na mortalidade pela doença na última década.
O VÍRUS C
A hepatite C é causada por um vírus esférico, envelopado e com uma cadeia única do tipo RNA pertencente à família Flaviviridae, a mesma da dengue e da febre amarela. Ele é muito diferente dos vírus que causam as outras hepatites mais comuns, a A e a B.
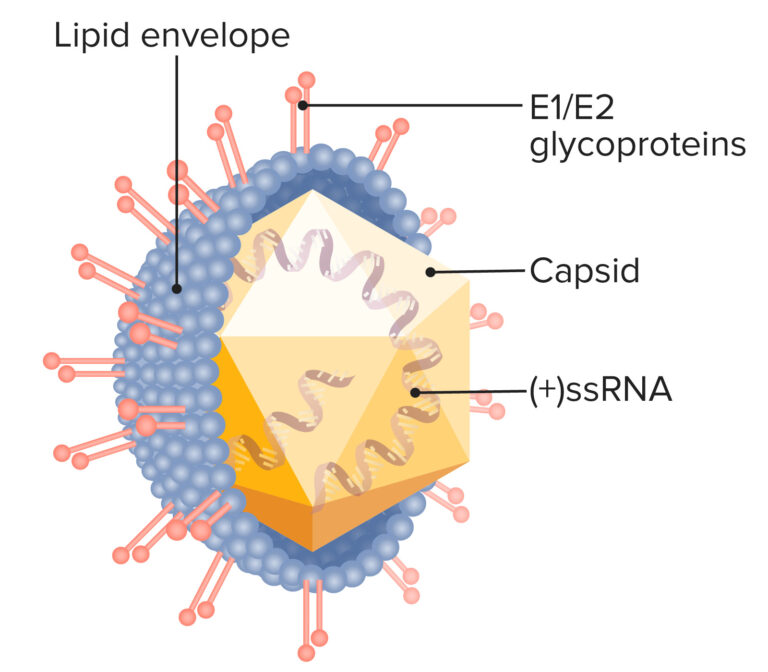

A variação genética entre os vírus da hepatite C é muito grande, o que faz com que alguns sejam mais ou menos agressivos e que tenham resposta diferente dependendo da medicação utilizada. Esses características justificaram dividir todos os vírus da hepatite C entre 6 genótipos (“famílias”) diferentes (de 1 a 6), e cada genótipo em dezenas de subtipos (1a, 1b, 2a, etc). Os genótipos chegam a apresentar 30 a 50% de diferença no seu RNA. Esta divisão é importante porque cada subtipo tem características próprias de agressividade e resposta ao tratamento. O mais comum é o genótipo 1, responsável por 40 a 80% das infecções, e que leva a doença mais severa e risco maior de hepatocarcinoma.
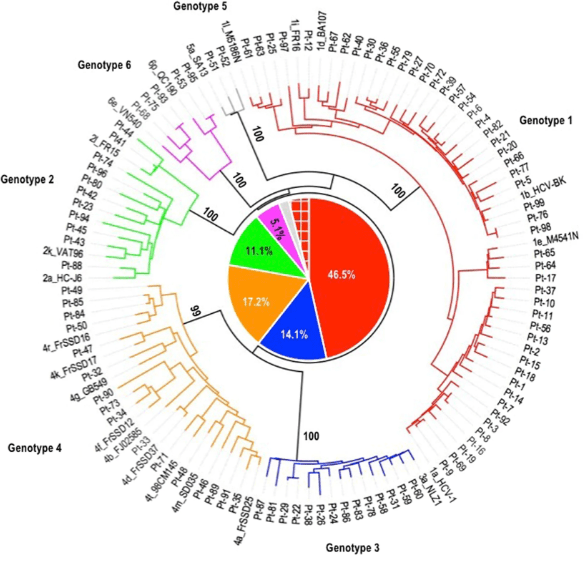
Essa diferença tão grande entre um vírus e outro dificulta muito a defesa do organismo, já que um anticorpo produzido contra um não vai proteger do próximo. É por isso também que até hoje não conseguimos produzir uma vacina eficaz para impedir a transmissão.
TRANSMISSÃO
A transmissão da hepatite C ocorre principalmente após o contato com sangue contaminado. O vírus da hepatite C chega a sobreviver de 16 horas a 4 dias em ambientes externos, o que facilita a infecção após contato com agulhas, material médico, odontológico ou de manicure contaminados. Grupos de maior risco incluem usuários de drogas endovenosas, pacientes em hemodiálise, homens homossexuais e trabalhadores da área de saúde.

A transmissão através de transfusões de sangue era uma das principais causas de novas infecções até 1992, quando foram desenvolvidos exames de rastreamento altamente eficazes, praticamente eliminando a possibilidade de se infectar com sangue. Hoje, a estimativa é de um caso de transmissão para cada 2 MILHÕES de unidades de sangue transfundidos.
Eliminando essa via, a principal forma de transmissão atualmente é pelo contato com sangue contaminado através de uso de seringas compartilhadas por usuários de drogas. Entre os usuários de drogas injetáveis mais jovens (18-30 anos), a incidência de hepatite C chega a um terço, enquanto que nos usuários mais velhos e ex usuários chega a 70-90%, reflexo da falta de cuidado da era pré AIDS. O uso de drogas inalatórias, como a cocaína, pode também levar a contato com sangue contaminado, pois causa hemorragia nasal e o canudo pode ser compartilhado, mas é mais difícil comprovar a transmissão por essa via.
A transmissão sexual é muito debatida. É verdadeiro que a hepatite C é muito menos transmitida sexualmente que a hepatite B. Em parceiros fixos de pessoas contaminadas, a prevalência de infecção é de apenas 0,4 a 3%, sendo que nesse muitas vezes encontramos outros fatores de risco que podem ser a causa da infecção. Por outro lado, entre pessoas sem nenhum outro fator de risco, encontramos 2 a 12% de sexualmente promíscuos. A relação sexual anal, no entanto, pelo contato com maior quantidade de sangue por lesão na mucosa, está relacionada a risco de transmissão e infecções recorrentes em homens homossexuais que fazem uso de profilaxia pré exposição para o HIV.
A transmissão vertical (mãe para filho) ocorre em 0 a 35,5% dos partos de mães infectadas, dependendo principalmente da quantidade de vírus circulante no momento do parto e se há coinfecção com HIV. A taxa de transmissão vertical em geral está entre 4,3 a 5,0%. Há aparente risco maior no parto normal que na cesariana e o aleitamento materno é seguro. Não há até o momento nenhuma técnica para reduzir o risco de transmissão para o bebê durante o parto, como é feito na hepatite B. Após o parto, deve ser realizada sorologia (anti-VHC) do bebê apenas após os 18 meses, pois antes disso os anticorpos detectados no sangue do bebê podem ser os provenientes do sangue da mãe, passados para o feto através da placenta. Há também a possibilidade de coleta de sangue para pesquisa do RNA VHC (pelo PCR) na primeira e na segunda consulta de puericultura (com o pediatra, entre um a dois meses de vida).

Outras formas de transmissão menos comuns são por agulhas usadas em acupuntura, agulhas (e tintas!) reutilizadas em tatuagem, equipamentos de manicure e pedicure e odontológicos não esterilizados. As normas sanitárias exigem uso de agulhas descartáveis e processos detalhados de esterilização de equipamento dentário, mas convém levar seu própria material para pedicure/manicure e exigir do tatuador não reutilizar frascos de tinta.
| Fatores de risco para o contágio da hepatite C |
| Transfusão de sangue ou derivados |
| Uso de drogas ilícitas |
| Hemodiálise |
| Exposição a sangue por profissionais da área de saúde |
| Receptores de órgãos ou tecidos transplantados |
| Recém-nascidos de mães portadoras |
| Contatos sexuais promíscuos ou com parceiros sabidamente portadores |
| Exposição a sangue por material cortante ou perfurante de uso coletivo sem esterilização adequada: procedimentos médico-odontológicos tatuagem acupuntura manicure / pedicure body piercing contato social ou familiar com material de uso pessoal ( barbeadores, escovas dentais, etc ) “medicina” folclórica ( inclui “cirurgias espíritas” ) barbeiros e cabelereiros |
Naturalmente, como tem os mesmos modos de transmissão, os portadores de hepatite C têm também um risco maior de outras doenças, particularmente a hepatite B a AIDS e outras doenças sexualmente transmissíveis, devendo realizar exames de sangue para diagnóstico. De particular interesse são a co-infecção hepatite B e C e hepatite C e HIV, com evoluções muito piores e tratamento mais difícil.
SINTOMAS
Diferente das hepatites A e B, a maioria (70-80%) das pessoas que adquirem a hepatite C desenvolvem doença crônica e lenta, sendo que a maioria (90%) é assintomática ou apresenta sintomas muito inespecíficos, como fraqueza crônica, dores musculares e articulares, cansaço, náuseas, prurido (coceira) ou desconforto no hipocôndrio direito.
Além dos sintomas relacionados diretamente à hepatite, o vírus pode desencadear o aparecimento de outras doenças através de estimulação do sistema imunológico:
| Manifestações extra-hepáticas do HCV | |
| Crioglobulinemia mista | Tireoidite autoimune |
| Porfiria cutânea tarda | Líquen plano |
| Glomerulonefrite membranoproliferativa | Sialoadenite |
| Poliarterite nodosa | Úlcera de córnea |
| Linfoma de células B | Síndrome de sicca |
| Fibrose pulmonar idiopática | Fenômeno de Reynaud |

Quando a hepatite C crônica progride para cirrose, podem surgir outros sintomas decorrentes da doença avançada, como ascite, icterícia, inchaço nas pernas, encefalopatia hepática ou hemorragia digestiva por varizes esofágicas.
HISTÓRIA NATURAL
A hepatite C aguda é assintomática em 84% dos casos, o que dificulta o diagnóstico. O tempo de incubação (entre o contato com o vírus até o desenvolvimento da hepatite aguda) é de 15 a 60 dias (média de 45 a 55 dias), mas a pessoa já pode transmitir a doença mesmo antes disso. Os sintomas mais comuns são icterícia, fadiga, febre, náusea, vômitos e desconforto em hipocôndrio direito, geralmente 2-12 semanas após a exposição e dura de 2 a 12 semanas. O diagnóstico da fase aguda requer a realização de PCR, uma vez que infecções agudas podem ser soronegativas.
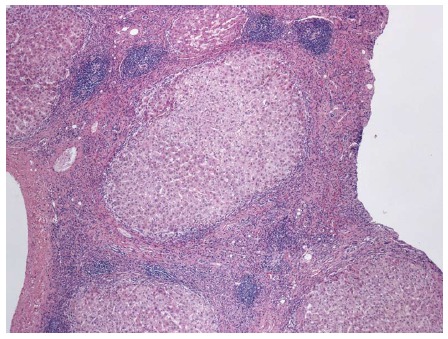
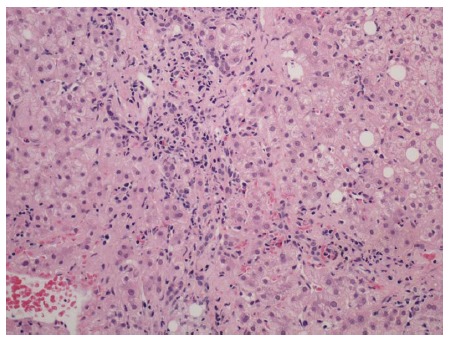
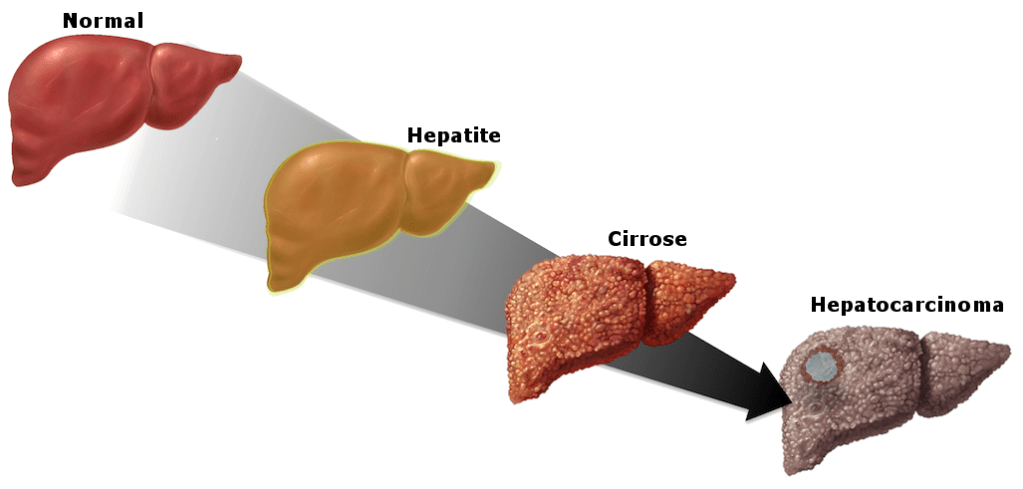
A principal diferença entre a hepatite C e as hepatites A e B é a sua alta cronicidade. Apenas 20 a 30% das pessoas infectadas pelo vírus da hepatite C curam espontaneamente, enquanto 70 a 80% ficam com hepatite crônica. Persistindo a doença, há destruição contínua das células do fígado pelo sistema imunológico e pelo próprio vírus. Como o fígado se regenera, as células destruídas continuam sendo repostas para manter a função do órgão, só que junto dessas novas células há a formação de cicatrizes, que vão se acumulando.

Com o ciclo contínuo de destruição de células e regeneração, o fígado vai acumulando cicatrizes com o passar dos anos. Na hepatite C crônica, em média a pessoa avança um estágio de fibrose a cada 7 a 10 anos, mas isso pode variar muito. Genótipos menos agressivos, como o 3, podem levar a doença mais lenta, enquanto que genótipo 1 e a presença de outros fatores, como álcool, obesidade, hemocromatose e infecção por outros vírus como o HIV e da hepatite B aceleram a progressão da doença.

A média (e isso varia muito) é que 20 a 30% dos portadores de hepatite C crônica chegarão ao estágio de cirrose entre 20 e 25 anos. A partir daí, há risco de progressão para cirrose avançada (sintomática) e câncer do fígado, mesmo que a hepatite seja tratada e curada. Daí a importância de diagnosticar e tratar a infecção o mais rápido possível.
Triagem
O principal método diagnóstico para a hepatite C continua sendo a sorologia para o anticorpo anti-HCV, que tem sensibilidade e especificidade superiores a 97% mas não consegue diferenciar entre hepatite aguda, hepatite crônica ou quem já está curando e mantém o anticorpo circulante. O mesmo acontece com os testes rápidos, que são os mais usados em campanhas. A recomendação hoje é que todo mundo deve realizar a sorologia pelo menos uma vez na vida, e quem tem fator de risco deve repetir a sorologia periodicamente.
A sorologia demora até 8 semanas para ficar positiva, portanto quando há suspeita de infecção aguda (após contato com sangue contaminado ou suspeito), deve-se repetir após o período de janela (tempo entre a contaminação e a sorologia positiva) ou realizar PCR se a suspeita for alta. Há maior risco de exame falso negativo em pessoas com o sistema imunológico comprometido, seja por uso de medicamentos, câncer, SIDA ou doença renal crônica ou em portadores de hepatite C com crioglobulinemia.
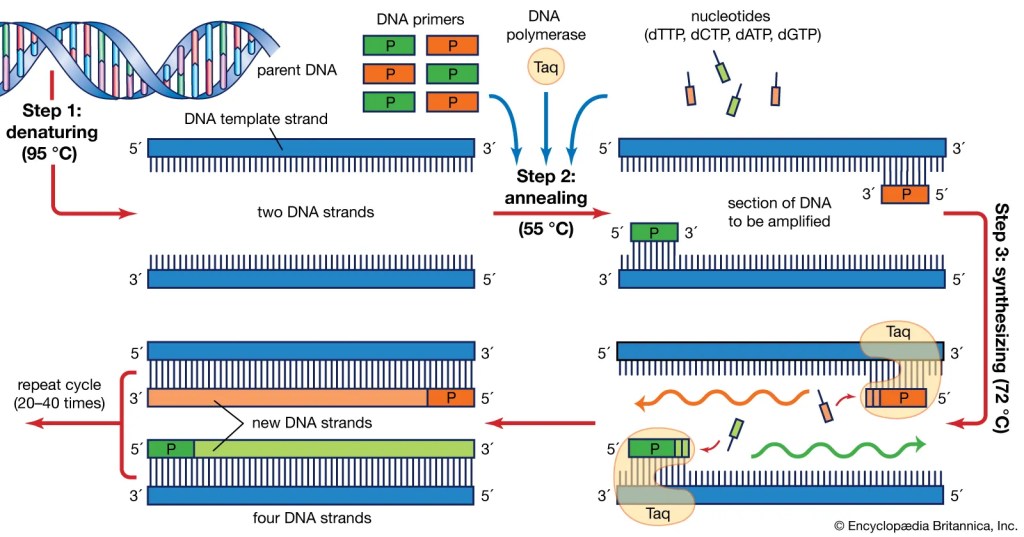
Confirmação
A confirmação da hepatite C vem através da reação de cadeia de polimerase (PCR), que detecta fragmentos do RNA do vírus na corrente sanguínea. O PCR pode ser usado na hepatite C em três formas distintas:
- PCR qualitativo, para demonstrar a presença de fragmentos do vírus no sangue (detecta quantidade mínimas). Pode ser usado para confirmar a hepatite C em pacientes com sorologia positiva, quando há necessidade de diagnóstico durante possível janela sorológica ou em quem tem suspeita de sorologia falso negativa por imunossupressão, doença renal crônica ou crioglobulinemia.
- PCR quantitativo, para medir a quantidade de vírus no sangue. Precisa de uma quantidade de vírus circulante maior que o teste qualitativo, e pode ser usado para verificar se a pessoa está respondendo ao tratamento (a quantidade de vírus diminui).
- Genotipagem, para definir de qual dos 6 genótipos (e dezenas de subtipos) é o vírus em questão. Isso pode ajudar a prever a evolução da doença, mas sua principal função é definir qual medicação e durante quanto tempo será o tratamento mais eficaz.

Exames adicionais
Confirmada a hepatite C, alguns exames adicionais são interessantes na prática. Primeiro, é necessário investigar a possibilidade de co-infecção de hepatite C com hepatite B ou HIV com as sorologias adequadas, para tratar essas doenças, mas também porque o tratamento da hepatite C pode ser diferente. Segundo, vale a pena dosar o hormônio tireoestimulante (TSH), pois cerca de 10% dos portadores de HCV podem desenvolver hipotireoidismo. E, finalmente, se o paciente tiver sinais de manifestações extra hepáticas da hepatite C (incluindo vasculite por crioglobulinemia), essas possibilidades devem ser investigadas. A elevação de transaminases não é necessária para o diagnóstico e não é mais condição exigida para o tratamento.
Estadiamento
O próximo passo é saber em que estágio está a doença do fígado. Como a hepatite C evolui lenta e silenciosamente, é importante saber se o portador do vírus já está ou não com cirrose, pois isso afeta o tipo de tratamento recomendado e o acompanhamento depois.
O ideal seria que todos fizessem um exame de imagem para avaliar o fígado, sendo que a ultrassonografia é simples, barata e disponível em praticamente qualquer lugar. Nem sempre dá para diagnosticar a cirrose baseado só em exame de imagem, mas é possível observar sinais sugestivos de cirrose hepática, hipertensão portal, esteatose ou hemocromatose e ainda encontrar lesões focais hepáticas (cistos, adenomas, hemangioma, câncer, etc.).
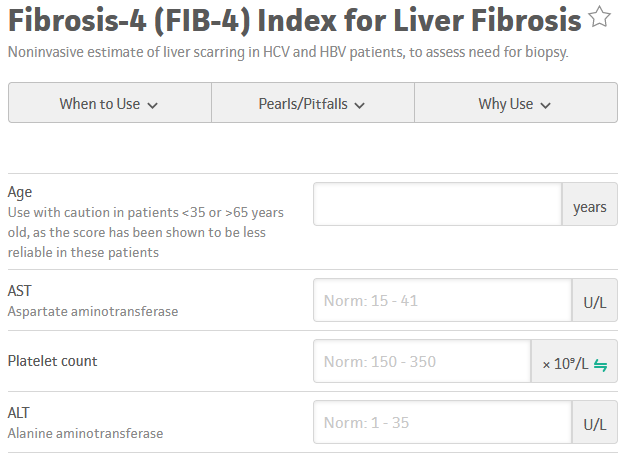
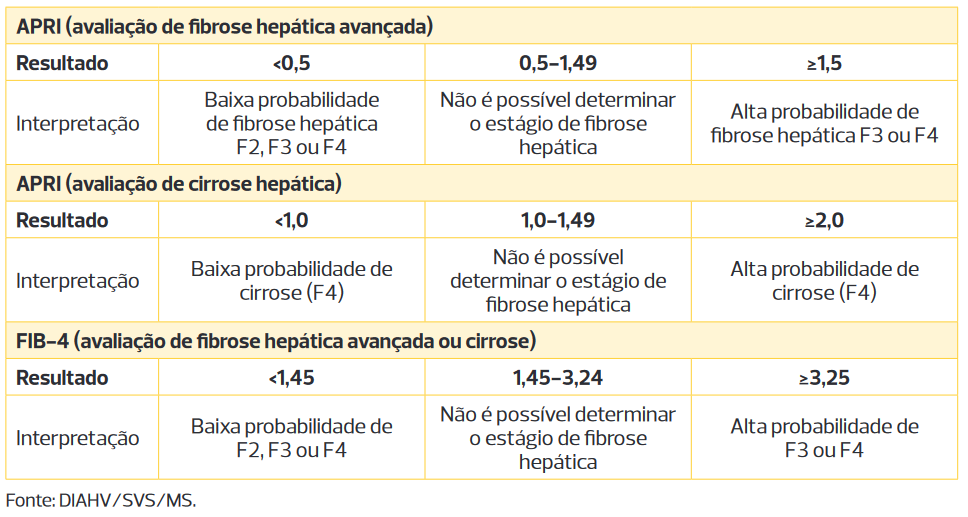
Como já discutimos acima, a hepatite C evolui lentamente do fígado normal para a cirrose, à medida que as cicatrizes vão se acumulando. Do ponto de vista prático, o que precisamos saber na hepatite C é se a pessoa já tem cirrose ou se não chegou nessa fase ainda. Para isso, o modo mais simples é realizar um escore não invasivo baseado nos exames que o portador da hepatite já tem. Há vários disponíveis, mas os mais simples são o FIB-4 e o APRI.
Se o APRI ou o FIB-4 são normais (APRI < 1,0 e FIB-4 < 1,45), isso praticamente descarta a possibilidade de cirrose. Se estão alterados, o próximo passo é realizar um segundo teste não invasivo, como a elastografia hepática, seja ela ultrassônica ou transitória (Fibroscan). Esses são exames que hoje estão amplamente disponíveis e substituem a biópsia hepática.
Hoje em dia não precisamos mais da biópsia nem para confirmar, nem para estadiar nem para conseguir liberação de medicamentos (no Brasil, o Sistema Único de Saúde fornece o tratamento gratuitamente). Ela atualmente é solicitada apenas em casos de dúvida diagnóstica, como em casos onde há dúvida se a lesão predominante do fígado é pela hepatite C, B ou HIV (nas coinfecções) ou quando há a possibilidade de outra doença, como a hepatite autoimune.
Exames de imagem, como ultrassonografia, tomografia ou ressonância magnética, são muito bons para avaliar a presença de nódulos no fígado e devem ser sempre solicitados, mas não são bons para dizer em cada estágio a doença está. Quando a cirrose é avançada podem ser vistos achados típicos, além de sinais de hipertensão portal e ascite, mas a cirrose em fase inicial pode passar despercebida pelos exames radiológicos.
CUIDADOS
Não há uma dieta específica que ajude ou prejudique o portador da hepatite C, mas deve-se evitar que a lesão do fígado pelo vírus seja potencializada por outros fatores, como obesidade, síndrome metabólica, álcool e uso de outras substâncias tóxicas ao fígado, como certos medicamentos (especialmente anti inflamatórios) e maconha. Não há nada que justifique repouso, o ideal é manter atividade física regular e dieta saudável.
| Dieta Saudável (Canadian Guidelines for Health Care Providers) |
|---|
| Alimentos variados contendo os quatro grupos principais (grãos, frutas e vegetais, leite e derivados e carne e/ou alternativas) |
| Ingesta adequada (não excessiva), distribuída ao longo do dia |
| Ingesta adequada de proteínas, para combater a infecção e permitir regeneração do fígado |
| Boa quantidade de frutas e vegetais para reduzir o dano pelos radicais livres no fígado (procure maior variação de cores) |
| Alimentos ricos em vitaminas A e C |
| Abstinência alcoólica |
| Limitar alimentos com excesso de gordura e açúcar |
| Balancear a dieta com atividade física, dentro das limitações necessárias |

Outra preocupação é em relação à transmissão. Recomenda-se que familiares e parceiros façam o teste. Se for mulher e estiver planejando engravidar, é melhor esperar o final do tratamento. Apesar do risco baixo, recomenda-se não compartilhar escovas de dente e lâminas de barbear. O risco de transmissão sexual é baixo, mas recomendo o uso de preservativos, especialmente no sexo anal. Usuários de drogas injetáveis devem usar agulhas e seringas descartáveis e descartar esses materiais em recipientes adequados.
TRATAMENTO
O tratamento da hepatite C avançou tanto nas últimas duas décadas, quando esse texto foi escrito pela primeira vez, que achei melhor apagar toda essa parte e começar de novo. Antes os medicamentos eram pouco eficazes e causavam uma infinidade de efeitos colaterais, tanto que os pacientes frequentemente comparavam o tratamento da hepatite C com quimioterapia por câncer. Era tão ruim que escolhíamos tratar apenas os que tinham doença mais severa (com mais inflamação ou fibrose) e observar os demais. Isso porque os medicamentos (o mais utilizado era o interferon alfa na versão normal ou peguilada) estimulava o sistema imunológico a destruir as células contaminadas. O efeito do tratamento, portanto, era indireto, e acabava levando a sintomas como perda de cabelo, febre e dor muscular, além de aumentar o risco de doenças autoimunes, como hipotireoidismo e diabetes.
Hoje os tratamentos atingem até 95% de chance de cura da hepatite (o que chamamos de resposta virológica sustentada – RVS, confirmada com um PCR negativo após 3 meses do final do tratamento). Ao contrário do interferon, que não atuava no vírus em si, agora usamos medicamentos que afetam diferentes partes do processo de multiplicação do vírus. Por isso chamamos esses de agentes de ação direta (AAD).
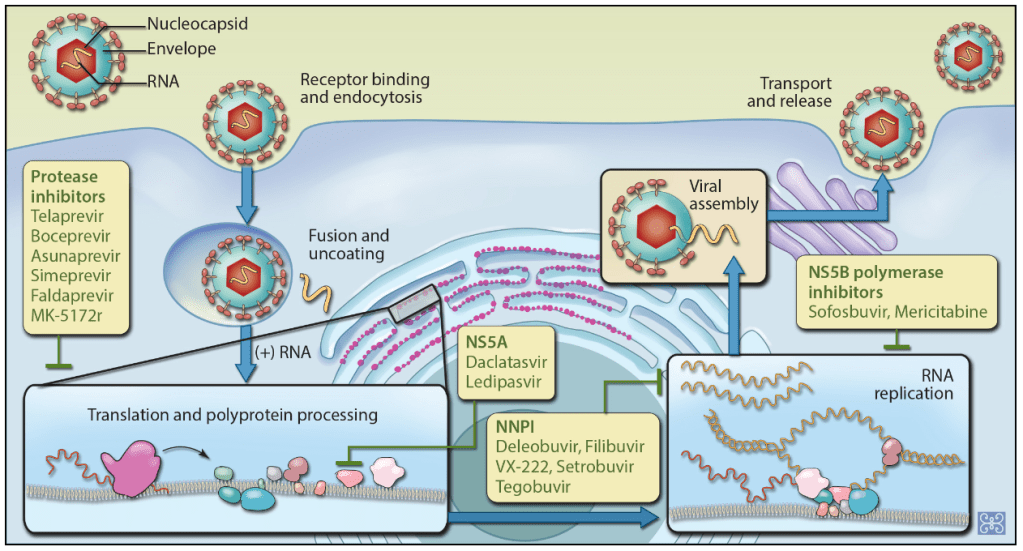
Alguns esquemas são mais curtos que outros e uns remédios funcionam melhor para determinado genótipo que para outro. Mas, graças ao esforço mundial em eliminar a epidemia de hepatite C (ver abaixo), a tendência está em oferecer para a população (já que no Brasil temos o direito de receber o tratamento gratuitamente pelo SUS) o esquema mais curto, eficaz e fácil de tomar possível e para TODOS, independente da intensidade ou do estágio da doença.
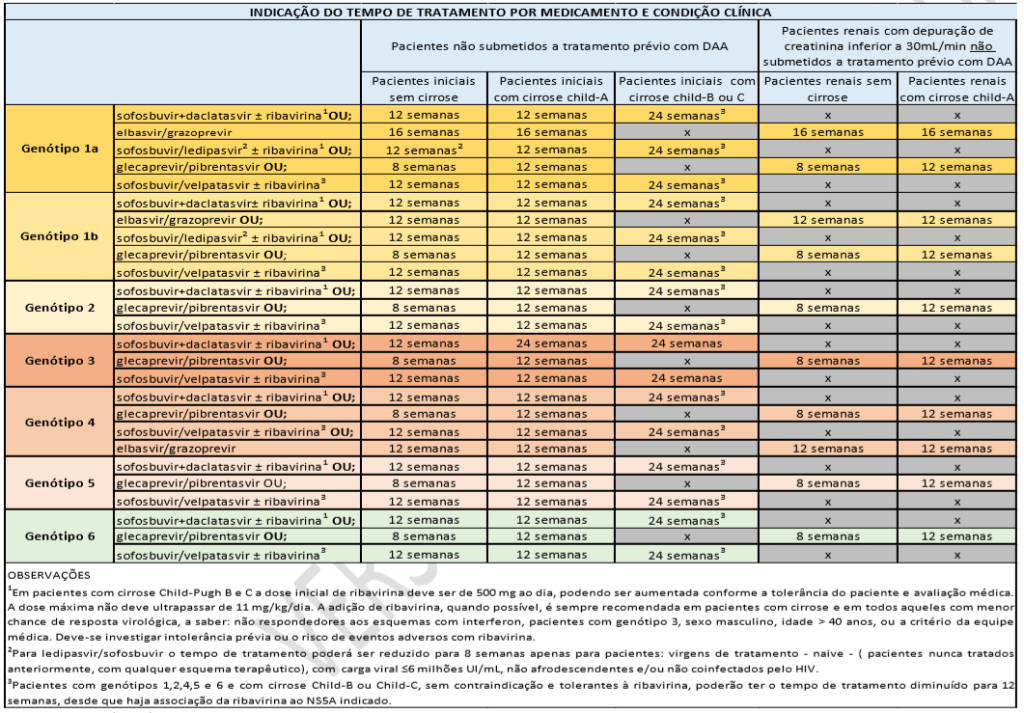
Discutir cada opção de tratamento é contraproducente, uma vez que os tratamentos disponíveis pelo SUS podem mudar rapidamente mais por questões de preço e disponibilidade do que técnicas. De modo geral, trata-se de um a dois comprimidos por dia, independente do genótipo (o que chamamos de tratamentos pangenotípicos) por 12 semanas se o portador não tiver cirrose ou se ela está na fase inicial (Child Pugh A). No caso de portadores com cirrose mais avançada (Child Pugh B ou C), recomenda-se tratar por 24 semanas ou associar com ribavirina e tratar por 12 semanas.
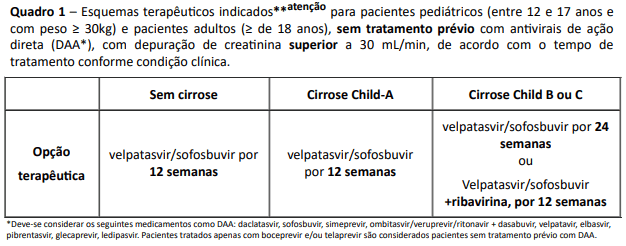
Efeitos colaterais são raros, sendo o mais comum a anemia pela ribavirina. É costumeiro fazer exames laboratoriais e rever o portador no meio do tratamento, para descartar efeitos colaterais e checar a aderência ao tratamento. Não se recomenda mais fazer o PCR durante o tratamento porque se estiver negativo não vai suspender o tratamento antes, e se der positivo não significa que não vai curar mais para frente. O PCR só é colhido antes e 12 semanas após o final do tratamento, quando se der negativo consideramos como resposta virológica sustentada (RVS), ou seja, cura.
O transplante de fígado é o tratamento de escolha para a hepatite C aguda fulminante (embora rara), crônica em fase de cirrose avançada (com encefalopatia hepática, ascite refratária, hemorragia digestiva de difícil controle por varizes e/ou episódio de peritonite bacteriana espontânea) ou na presença de hepatocarcinoma.

A indicação de transplante na hepatite C depende, portanto, das condições do fígado, não da hepatite C. A hepatite C deve ser tratada antes do transplante se possível, se não for trata-se após o transplante. Hoje até aceitamos que o doador do fígado pode ter hepatite C, desde que o fígado ainda esteja em boas condições.
PÓS TRATAMENTO
Após o tratamento e a demonstração de RVS, não há necessidade de acompanhamento médico, EXCETO nos casos de risco para outras doenças (drogadição, coinfecção com HIV, etc.) e nos portadores de cirrose. Mesmo que a fibrose do fígado melhore e até os exames de imagem e de sangue voltem ao normal, sabemos que o risco de desenvolver hepatocarcinoma persiste, e devemos realizar reavaliação médica com um exame de imagem e exames laboratoriais a cada 6 meses por toda a vida.
O COMBATE À PANDEMIA
Em 2016, os países membros da Organização Mundial da Saúde assumiram o compromisso de controlar globalmente a epidemia das hepatites virais até 2030. O objetivo final, segundo a proposta, era de reduzir em 90% o número de novas infecções e em 65% o número de mortes causadas por hepatites virais entre 2022 e 2030. Esse acordo foi firmado por ser possível, já que temos toda a tecnologia necessária para o diagnóstico de portadores e de bolsas de sangue, vacinas para as hepatites A e B, tratamento curativo altamente eficaz para a hepatite C e que controla adequadamente a hepatite B.

Segundo o acordo, os objetivos seriam atingidos pela implementação de 5 intervenções principais:
- vacinação de crianças contra a hepatite B
- prevenção da transmissão vertical (de mãe para filho) da hepatite B
- segurança no sangue e injeções
- reduzir risco para usuários de drogas injetáveis
- testar o maior número possível de pessoas e tratar os infectados
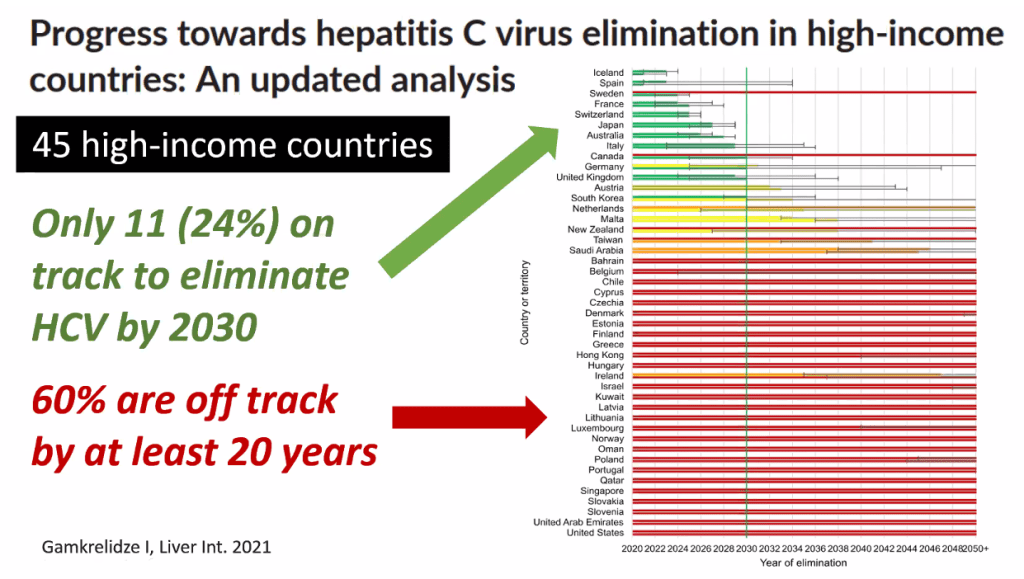
Infelizmente, e em parte pela pandemia, mas em grande parte pela falta de vontade política, os resultados são deprimentes: apenas 14 países aparentemente vão cumprir seus objetivos para a hepatite C, e nenhum para a hepatite B.
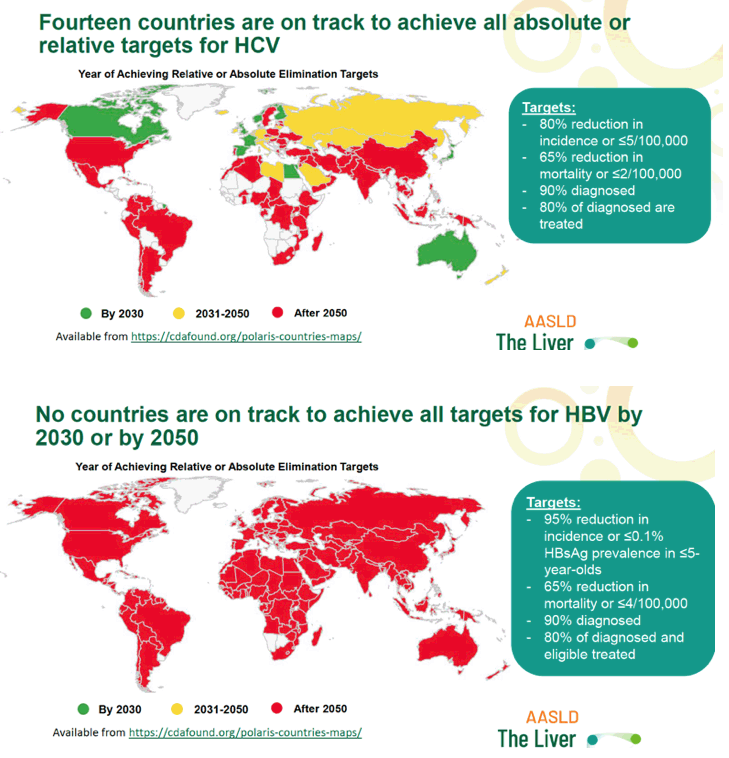
A previsão atual é que os demais países, incluindo o Brasil, não só não vão atingir esses objetivos até 2030, como provavelmente não vão conseguir até 2050 também. Quantos milhões de pessoas vão ficar doentes e morrer por causa disso ?
Temos todas as ferramentas nas mãos, o que falta é colocá-las em prática. O governo tem grande responsabilidade sobre isso, mas não pode fazer tudo sozinho. Temos que fazer um esforço em conjunto do Governo, dos serviços de saúde e da população. Não adianta ter prateleiras cheias de remédios e testes de hepatite se as pessoas não vão fazer os exames. O primeiro passo é chamar atenção para o problema, assim divulgue ! Se não fez ainda, faça exames ! Cobre os políticos sobre ações concretas, mas faça também sua parte !
BIBLIOGRAFIA
- Rodriguez, C., Soulier, A., Demontant, V. et al. A novel standardized deep sequencing-based assay for hepatitis C virus genotype determination. Sci Rep 8, 4180 (2018). https://doi.org/10.1038/s41598-018-22614-0
- Bonkovsky HL, Mehta S. Hepatitis C: a review and update. J Am Acad Dermatol. 2001 Feb. 44(2):159-82.
- Aguiar MF, Faria-Janes AL, Garcia-Brandes GI, Takemi-Emori C, Ferraz MLG, Andrade LEC, de Souza AWS. Prevalence of cryoglobulinemia and cryoglobulinemic vasculitis in chronically HCV-infected Brazilian patients. Ann Hepatol. 2019 Sep-Oct;18(5):685-692. doi: 10.1016/j.aohep.2019.04.010. Epub 2019 May 21. PMID: 31167733.
- Charles ED, Dustin LB. Hepatitis C virus-induced cryoglobulinemia. Kidney Int. 2009 Oct;76(8):818-24. doi: 10.1038/ki.2009.247. Epub 2009 Jul 15. PMID: 19606079; PMCID: PMC2755598.
- Britannica, The Editors of Encyclopaedia. “polymerase chain reaction”. Encyclopedia Britannica, Invalid Date, https://www.britannica.com/science/polymerase-chain-reaction. Accessed 31 August 2023.
- Ministério da Saúde. Protocolo Clínico e Diretrizes Terapêuticas para Hepatite C e Coinfecções 2019. Última modificação: 31.08.2020 (link)
- Dhingra S, Ward SC, Thung SN. Liver pathology of hepatitis C, beyond grading and staging of the disease. World J Gastroenterol. 2016 Jan 28;22(4):1357-66. doi: 10.3748/wjg.v22.i4.1357. PMID: 26819505; PMCID: PMC4721971.
- OFÍCIO CIRCULAR Nº 6/2022/CGAHV/.DCCI/SVS/MS 14/02/2022 (link)
- Sanjiv, C e Pockros PJ. Overview of the management of chronic hepatitis C virus infection. UpToDate acessado em 16/09/23 (link)
- Au JS, Pockros PJ. Novel therapeutic approaches for hepatitis C. Clin Pharmacol Ther. 2014 Jan;95(1):78-88. doi: 10.1038/clpt.2013.206. Epub 2013 Oct 14. PMID: 24126682.
- Debika Bhattacharya, Andrew Aronsohn, Jennifer Price, Vincent Lo Re, the American Association for the Study of Liver Diseases–Infectious Diseases Society of America HCV Guidance Panel , Hepatitis C Guidance 2023 Update: American Association for the Study of Liver Diseases– Infectious Diseases Society of America Recommendations for Testing, Managing, and Treating Hepatitis C Virus Infection, Clinical Infectious Diseases, 2023;, ciad319, https://doi.org/10.1093/cid/ciad319
Artigo criado em: 2003
Última revisão: 17/09/2023